






投资管理
你现在的位置:首页 > 投资管理 > 投资管理投资人必读:药企的基因战争(转型的阵痛才刚刚开始)
来源:医药投资并购俱乐部 作者:罗奇斌 发布时间:2017-03-28 点击数:4024次
前情提要
据网易财经报道,中国已是全球第二大医药市场国家,目前我国有近5000家药企,其中九成以上为仿制药企业。我国的药品审批改革在酝酿了十余年以后,在2015年这个关键的时间节点,终于出手了。这个“投资人必读系列”,通过每一个连载故事(第二十二系列:药企的基因战争),把读者带入一个大健康领域。这个系列作为投资人入门级别的行业必读知识,希望能够给中国投资界一盏小小的明灯。
国内药企九成以上为仿制药企业
据网易财经报道,中国已是全球第二大医药市场国家,国内仿制药市场规模在今年或接近5000亿元。目前我国有近5000家药企,其中九成以上为仿制药企业。 根据食药总局提供的统计数字,中国已有的药品批准文号总数高达18.9万个,95%以上为仿制药。
然而全球最大的仿制药战场还是在美国,据IMS统计,2013年全球仿制药市场规模达到1600亿美元中,美国就占到了500亿美元。作为排在全球第二的中国,每年专利药专利到期是仿制药市场增长的主要动力,预计全球在未来三年平均每年到期的专利药市场规模能达到300亿美元。
在中国近5000家药企里面,200亿市值以上的企业有25家,100亿-200亿市值的企业有49家,50亿-100亿市值的企业为68家。 在过去几年中,中国对制药行业的研发投资从2001年的1.62亿美元增加至2011年的32.5亿美元。美国的前十企业的市场集中度达到50%以上,大部分仿制药批文掌握在这些大型仿制药企业手中。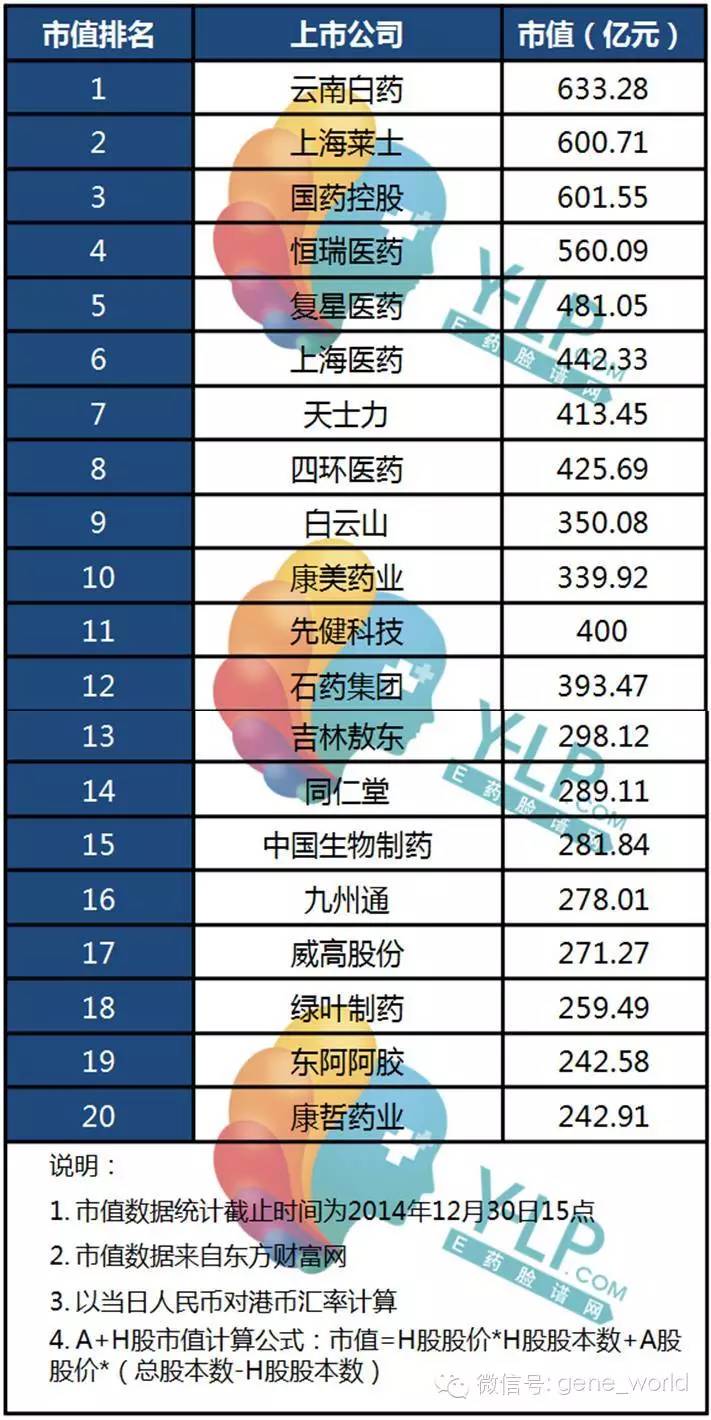
在我国药品可以分为新药和仿制药。所谓的仿制药,简单来理解就是仿已有国家标准的药品。在8月18日国务院的《关于改革药品医疗器械审评审批制度的意见》正式出台以后,这一条标准已经调整为“仿与原研药品质量和疗效一致的药品”。
仿制药比重在中国高居不下,这与创新药研发的高额成本是分不开的。美国塔夫茨大学药物开发研究中心的一项数据显示,开发一个新药的平均成本大约为26亿美元。2013年,中国前十强药企的研发投入仅为销售额的1%,和全球前十强药企的研发占比率17.8%相比,这个数字并不乐观。
“研发新药时间长,费用达,而且推广上市成功率低,不如仿制药成本低、风险小,资金回笼快。这是我国药企扎堆仿制药的根本原因。”一位药企业内人士对时代周报记者如此的描述。
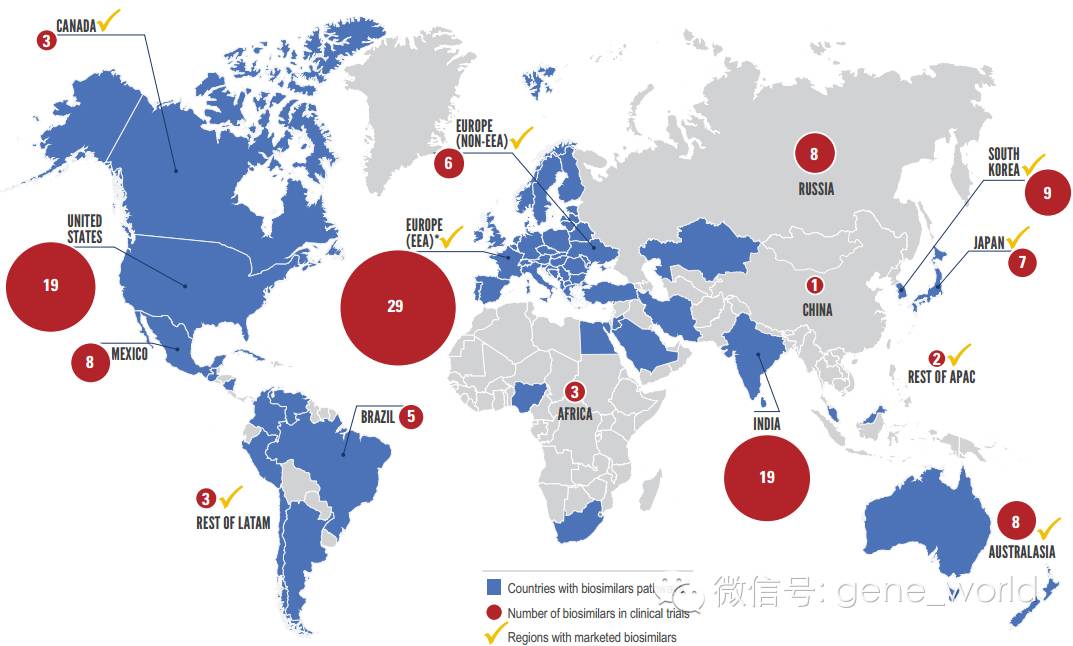
中国的大健康产业要启航,健康产业未来要走出国门,医疗体制改革势在必行。要解决“看病难、看病贵的问题”,首先需要在药品和医疗服务上面“动刀”和“换血”。这里的“动刀”,便是对药品的审批提高门槛,对药品的价格进行调控。
中国的药企格局严重失调,生产同质化严重,注定要转型。九成以上的仿制药企业竞争激烈,药品的销量越来越不理想,利润越来越低,短时间内通过改进设备和提供工艺来提高竞争力不太现实,创新药的研发迟迟徘徊在摇篮里。企业需要找到出路。
中小型仿制药企业的出路会有两个方向,一个是“抱大腿”,也就是通过各种方式“挂靠”到大药企进行合作和发展;另一个是“谋转型”,通过提高研发能力和运用资本进行“换血”,达到转型的目的。药明康德新药开发有限公司首席技术官陈智胜表示,中国的医药市场目前处于群雄乱战的状态,但将来必定会走向“三国鼎立”;希望中国将来的格局是,有3-5大的仿制药企业,以及两三百家做创新药的企业。
要实现如此之格局,药企行业必将面临一场腥风血雨般洗牌,国家政策的推波助澜,会让这场风雨来得更快更猛。
政策推动药企形成格局
自从我国走上“有中国特色”的经济道路以来,各行各业都在摸索能够适应中国特有国情的改革之路。我国的药品审批改革在酝酿了十余年以后,在2015年这个关键的时间节点,终于出手了。
中国的经济改革几十年,我们的政府越来越熟练的运用宏观调控这个杠杆,也越来越高明的打出政策这张王牌。2015年首先打出的两张王牌,便是专利许可和药品审批。
企业的命脉离不开价格,对价格的调控是政府从经济改革以来一直在使用的政策王牌,然而价格这把“双刃剑”离开了市场的调控往往会产生联动效应。政府在打出这张牌之前,往往是先布局。对药品定价的调控,考验的不仅仅是政府的经济手腕,还牵连到和国际药企巨头们的周旋。
在药品定价上面,政府首先走出了“专利许可”这一步棋。第一招是政府通过国家知识产权局对进口创新药的专利申请进行严审。严审达到的效果是通过宣布申请专利无效来推动国内仿制药企业和国外药企达成协议,实现原研药在国内的仿制。第二招是签发“专利强制许可证”,实现国内药企合法仿制。这两招都能降低药价,部分缓解“吃药贵”的问题。
2015年6月26日,国家知识产权局向《财经》记者证实,在数月前国家知识产权局驳回了美国吉利德公司(Gilead Science)对索菲布韦关键专利申请的消息,吉利德公司在收到驳回信息后立即提出复审,该局将在三个月内给出复审意见。
索菲布韦是什么药物呢?美国吉利德公司又是何方神圣?
索非布韦(又译为索氟布韦,英文名Sofosbuvir,商品名Sovaldi)是吉利德公司开发用于治疗慢性丙肝的新药,于2013年12月6日经美国食品药品监督管理局(FDA)批准在美国上市,2014年1月16日经欧洲药品管理局(EMEA)批准在欧盟各国上市。
这款由吉利德公司研发的新药,是首个无需联合干扰素就能安全有效治疗某些类型丙肝的药物,在治疗1型、2型和4型丙肝时,索菲布韦联合其他药物的临床治愈率高于90%,并且没有传统治疗方案产生的流感样症状、血细胞减少、精神异常、自身免疫性疾病、肾脏损害等副作用。此外,索非布韦的临床试验还包含了一些丙肝转成肝硬化的患者,疗效也较显着。
目前,索非布韦还未在中国上市。
在美国,丙肝经常漏诊,丙肝病毒影响大约320万美国人,每年约15,000人死亡,主要死于肝硬化与肝癌。按照吉利德公司发言人Cara Miller的说法,大部分病人需要应用这种每天花费在1000美元的药物治疗12周,总花费约84,000美元。根据独立分析公司Datamonitor Healthcare发布的报告,在未来9年,丙型肝炎(Hepatitis C)市场预计将增长230%,并在2022年达到155亿美元。
索菲布韦在美一个疗程8.4万美元、一片药剂约1000美元,在美国购药治疗的患者彻底治愈将花费近100万元人民币,对于国内的患者家庭来说,这无疑是一个天价。英国利物浦大学一个研究组的研究显示,索菲布韦每粒药丸的生产成本仅是1美元,整个疗程的生产成本约为101美元。
在我们的邻国印度,对待这样的天价进口药,政府是如何应对的呢?
印度专利部门直接拒绝了索菲布韦的关键专利申请,包括前药与基础化合物的专利。2014年9月,吉利德公司转而与印度七家仿制药巨头签订非独占特许权协议。根据协议,七家印度厂商可获得吉利德的完整技术转让,自主生产索非布韦并自行定价。拥有自主定价权的印度药企,将仿制药的药价定为一个疗程900美元左右。索菲布韦印度仿制药的药效与原研药相差无几。印度药企有权将该仿制药分销至全球91个国家,但不包括中国。
中国政府尝试走一条“印度式”的道路,但是这样的“好事”能否在中国再度复制呢?即便吉利德公司的前药专利申请最终没能通过,中国药企也难以实现像印度药企一样的合法仿制。国家知识产权局网站显示,吉利德公司已经掌握索菲布韦的基础化合物专利,该专利的状态为“专利权维持”,于2024年4月21日到期。
鉴于中国特殊的药品审核制度,索菲布韦原研药与印度仿制药注定无法在中国“登陆”。政府的第一招“专利申请审核”能否推动国内5000家药企合法仿制呢?从国家知识产权局网站显示,已经有不少于九家国内药企提交了索菲布韦制剂的专利申请。
然而,仿制药的研发也不是轻易能够完成的。由于吉利德公司掌握了关键专利,国内药企合法生产仿制药这条路基本上是行不通的,只能退而走生产“me-too”药。”me-too”药是药企为了避开专利药物的产权保护而以现有的药物为先导物进行研发的、具有自己知识产权的药物。但是这种仿制药在药效上和原研药会有很大的差别,不同实力的药企由于生产工艺的良莠不齐,最终生产出来的仿制药在药效上也会大打折扣。
一旦这样的情况发生,政府就不得不使用“专利许可”这张王牌的第二招:“专利强制许可”。专利药品强制许可,被视为解决公共健康危机与专利药品昂贵矛盾的一剂良方。
世贸组织的《与贸易有关的知识产权协议》规定,成员国发生公共健康危机,如艾滋病、疟疾、肺结核和其他流行疾病时,可考虑实施药品专利强制许可,仿制生产仍在专利期限内的药物来解决公众危机。
一旦使用这一招,专利在行政干预下被放开,虽然能解决公共健康危机,但是势必会影响到具有创新药开发能力企业的积极性,助长仿制药企业的投机取巧,长远来看对于医疗行业发展是不利的。
美国卫生部在“9•11”事件后,曾因炭疽病毒引发的恐慌,将强制许可作为谈判砝码,迫使拜耳(Bayer)公司大幅度降低了治疗炭疽病毒的药品西普洛的价格。巴西、南非、泰国等国曾对治疗艾滋病等传染病的二线药物实施过强制许可。在2012年3月,印度政府批出了有史以来的第一个抗癌药物的强制许可,允许本土制药商生产德国制药商拜耳公司抗癌药物Nexavar的仿制版药物,最终使仿制药与原研药相比降价幅度达到97%。
《专利法》颁布30余年,中国未曾实施过一例专利强制许可。政府在使用这一招上面没有经验,国内药企尽管很欢迎政府启动专利强制申请,但是“屁股决定脑袋”的规律只能是让企业在无法等待的过程中,退而求“me-too”药的研发。没有一家药企敢于做“第一个吃螃蟹的人”给政府施加压力启动专利强制许可。
归根结底,这是国内药企的底气不足造成的。不到一成的创新药企业,不超过1%的研发投入,造成了我国的药企格局严重失调。如果说政府的第一张王牌“专利许可”打出了对药价的宏观调控效果,下一个要打出的王牌“药品审批”,便是直指仿制药企业的“七寸命脉”。
2015年7月22日,国家食药总局发布了《关于开展药物临床试验数据自查核查工作的公告(2015年第117号)》;7月31日晚再发文《关于征求加快解决药品注册申请积压问题的若干政策意见的公告(2015年第140号)》,提出了提高仿制药审批标准、严惩注册申报造假行为、退回不符合条件的注册申请等十条措施,被业内称为“最严药品评审令”。
8月18日,国务院出台《关于改革药品医疗器械审评审批制度的意见》。清华大学法学院院长、国家食药总局药品监管法规司顾问王晨光在接受时代周报记者采访时提到:“文件出台对中国的药品监管来说非常重要。它不仅是对我国未来药品质量标准的提高很重要,未来也将导引药品审评、审批、药品上市许可等一系列配套制度的出台。最终还将直接影响整个药品行业的监管方式和监管模式的转变。”
这一系列药品监管的改革出台,直接的后果就是提高了仿制药门槛。对仿制药的质量标准提高,意味着仿制药企业的技术水平、制剂工业、制药设备及辅料等方面都需要改进和提升,这意味着成本的提升。同时在一致性评价或生物等效实验等方向的投入,也会让一些实力不足的企业面临转型的困难。
长痛不如短痛,中国的药企除了形成稳定格局,还肩负着走出国门的使命。这个使命承载着的是政府新一代年轻有野心的实力派的愿景,一种对医疗改革的决心和大健康产业走出国门的眼光。在政策不明朗的形势下,是否会再次上演企业改革中的“抓大放小”呢?改革路上能够获得“绿色通道”的药企是否“不负众望”实现转型呢?带着这些问题,药企们开始走上了一条“互联网+”和“基因+”的道路。